Ο ρόλος του ογκολόγου στον πρώιμο καρκίνο μαστού είναι μέγιστης σημασίας, καθώς εκείνος θα προσφέρει τις κατάλληλες επιλογές στην ασθενή.
Ειδικός Παθολόγος-Ογκολόγος, MD, PhD
Ο ρόλος του ογκολόγου στον πρώιμο καρκίνο μαστού
ΦΥΣΙΚΗ ΙΣΤΟΡΙΑ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ
Ο καρκίνος του μαστού θεωρείται, υποθετικά, νόσος διάσπαρτη, ακόμη και στα αρχικά της στάδια από κάποιους, έτσι ώστε ν’αντιμετωπιστεί αποτελεσματικότερα.
Η τοπική θεραπεία, δηλαδή η χειρουργική, δεν αποκλείει την υποτροπή τοπική ή απομακρυσμένη.
Παρόλα αυτά, μεγάλος αριθμός γυναικών ζουν χωρίς συμπτώματα της νόσου και πεθαίνουν από άλλη αιτία.
Ο ΡΟΛΟΣ ΤΟΥ ΟΓΚΟΛΟΓΟΥ ΣΤΟΝ ΠΡΩΙΜΟ ΚΑΡΚΙΝΟ ΤΟΥ ΜΑΣΤΟΥ
Ο ογκολόγος έχει ως στόχους την προεγχειρητική συστηματική θεραπεία (;) ή την επικουρική, δηλαδή τη μετεγχειρητική συστηματική θεραπεία (;).
Επίσης, αναλαμβάνει το έργο της παρακολούθησης και φυσικά της πρόληψης.
Συστηματική θεραπεία πρώιμης νόσου
Προεγχειρητική (Neoadjuvant) (;) Καλύτερα να μη γίνεται
Στόχοι της προεγχειρητικής θεραπείας είναι να διευκολύνει τη χειρουργική αφαίρεση του πρωτοπαθούς όγκου, επιτρέποντας συντηρητικότερες επεμβάσεις με διατήρηση του μαστού, να μειώσει τη θνητότητα της νόσου, αυξάνοντας την ελεύθερη νόσου επιβίωση και την ολική επιβίωση και να επιτρέψει τη μελέτη της βιολογίας της νόσου και την ανταπόκριση στη θεραπεία, οδηγώντας, έτσι σε αποτελεσματικότερες και εξατομικευμένες θεραπευτικές στρατηγικές (πρέπει πάντα να γίνεται σύμφωνα με το μοριακό προφίλ του όγκου και όχι τυχαία).
-Υποψήφιες για προεγχειρητική χημειοθεραπεία είναι οι γυναίκες με μη μεταστατικό καρκίνο του μαστού, στις οποίες δεν είναι δυνατή η συντηρητική χειρουργική επέμβαση με διατήρηση του μαστού και των οποίων ο όγκος έχει χαρακτηριστικά αυξημένης χημειοευαισθησίας:
- Χαμηλή ή μη έκφραση ορμονικών υποδοχέων.
- Χαμηλός βαθμός ιστολογικής διαφοροποίησης (ki67, MIB1/Mindbomb Homolog-1, S-phase/ σύνθεση DNA/ σύνθεση Deoxyribonucleic acid/σύνθεση Δεοξυριβονουκλεϊκού οξέος).
- Υψηλός δείκτης πολλαπλασιασμού.
- Ο μη λοβιακός διηθητικός ιστολογικός τύπος (Luminal B, Triple negative, HER2 +).
Ως προεγχειρητική ΧΜΘ χρησιμοποιούνται, σήμερα, συνδυασμοί ανθρακυκλίνης και ταξάνης. Αν υπάρχει υπερέκφραση ή ενίσχυση HER2 πρέπει να συγχορηγείται το μονοκλωνικό αντίσωμα trastuzumab (προσοχή στην καρδιοτοξικότητα). Χορηγούνται τουλάχιστον 6 κύκλοι ΧΜΘ. Εκτίμηση της ανταπόκρισης γίνεται σε 6-9 εβδομάδες.
Πατήστε, εδώ, για να διαβάσετε για τη τραστουζουμάμπη και τις παρενέργειές της
Αν δεν υπάρχει ανταπόκριση, γίνεται άμεσα χειρουργική επέμβαση ή αν υπάρχει χρονικό περιθώριο δοκιμάζεται άλλο σχήμα.
Εκτίμηση ανταπόκρισης γίνεται με: τη φυσική εξέταση, το υπερηχογράφημα μαστών και την MRI/Magnetic Resonance Imaging/Απεικόνιση μαγνητικού συντονισμού ή FDG-PET scan/18-Fluoro-deoxyglucose positron emission tomography/Τομογραφία εκπομπής ποζιτρονίων 18-φθορο-δεοξυγλυκόζης.
Σκοπός της προεγχειρητικής ΧΜΘ είναι η επίτευξη παθολογοανατομικής πλήρους ύφεσης στο διηθητικό και μη διηθητικό στοιχείο, τόσο στο μαστό, όσο και στους μασχαλιαίους λεμφαδένες δεδομένου, ότι σε αυτούς τους ασθενείς, το DFS/ Disease-free survival (ελεύθερη νόσου επιβίωση) και το OS/overall survival (ολική επιβίωση) είναι καλύτερα από ότι στη μη πλήρη ανταπόκριση.
–Υποψήφιες για προεγχειρητική ορμονοθεραπεία είναι οι γυναίκες με μη μεταστατικό καρκίνο του μαστού, στις οποίες δεν είναι δυνατή η συντηρητική χειρουργική επέμβαση με διατήρηση του μαστού και των οποίων ο όγκος έχει χαρακτηριστικά μειωμένης χημειοευαισθησίας:
- Υψηλή έκφραση ορμονικών υποδοχέων.
- Υψηλός βαθμός ιστολογικής διαφοροποίησης (ki67, MIB1, S-phase).
- Χαμηλός δείκτης πολλαπλασιασμού.
- Ο λοβιακός διηθητικός ιστολογικός τύπος (Luminal A).
Η διάρκεια είναι 4-6 μήνες με χαμηλά ποσοστά πλήρους ανταπόκρισης 1%-8%. Η προεγχειρητική ορμονοθεραπεία σε μεταεμμηνοπαυσιακές γυναίκες γίνεται με αναστολείς αρωματάσης ή ταμοξιφαίνη, ενώ για την προεγχειρητική ορμονοθεραπεία σε προεμμηνοπαυσιακές γυναίκες υπάρχουν λίγα δεδομένα.
Συγκρίνοντας τη neoadjuvant, έναντι της adjuvant θεραπείας, από μια μετα-ανάλυση 9 τυχαιοποιημένων μελετών, που δημοσιεύτηκε το 2005 βρέθηκε, ότι η neoadjuvant και η adjuvant θεραπεία πρέπει να θεωρούνται, ότι έχουν κλινικά ισοδύναμη αποτελεσματικότητα και η χειρουργική αφαίρεση του πρωτοπαθούς όγκου δεν πρέπει να παραλείπεται σε ασθενείς, που υποβάλλονται σε προεγχειρητική χημειοθεραπεία.
Συστηματική θεραπεία πρώιμης νόσου Επικουρική (Adjuvant)
ADJUVANT (Συστηματική Θεραπεία Μετεγχειρητικά)
- Ορμονοθεραπεία.
- ΧΜΘ +/- trastuzumab
Σκοπός της, είναι η εξαφάνιση της μικρομεταστατικής νόσου και η αύξηση του DFS (Disease Free Survival). Ο ρόλος της συμπληρωματικής χημειοθεραπείας είναι η καταστροφή των καρκινικών κυττάρων, που θα μπορούσαν να έχουν διαφύγει και η παράταση του χρόνου εμφάνισης τυχόν υποτροπής. Η μετεγχειρητική συμπληρωματική θεραπεία μπορεί να είναι χημειοθεραπεία, ορμονοθεραπεία, Trastuzumab ή συνδυασμός τους.
-Όταν η θεραπευτική απόφαση έχει σχέση με την ύπαρξη ή όχι εμμήνου ρύσεως
Στις προεμμηνοπαυσιακές γυναίκες, χορηγείται χημειοθεραπεία και ορμονοθεραπεία και (LHRH ανάλογα/Luteinising Hormone Releasing Hormone ανάλογα/Ορμόνη απελευθέρωσης ωχρινοτρόπου ορμόνης), αντί της ωοθηκεκτομής.
Στις μεταεμμηνοπαυσιακές γυναίκες χορηγείται ορμονοθεραπεία με ή χωρίς χημειοθεραπεία.
Όπως υποστηρίζουν αυτοί, που έχουν βγάλει τις κατευθυντήριες οδηγίες, η πολυχημειοθεραπεία έναντι καμιάς θεραπείας μειώνει τον κίνδυνο υποτροπής και θανάτου. Το όφελος, αφορά όλες τις ηλικίες, αλλά θεωρείται σημαντικό σε ασθενείς μικρότερες των 50 ετών. Η απόλυτη μείωση του κινδύνου είναι μεγαλύτερη στους αρνητικούς ορμονικούς υποδοχείς (ER-), παρά στους θετικούς ορμονικούς υποδοχείς (ER+). Οι γυναίκες, με θετικούς λεμφαδένες (LN+) έχουν μεγαλύτερο απόλυτο όφελος από τις γυναίκες με αρνητικούς λεμφαδένες (LN–). Lancet 351: 1451, 1998
-Κατευθυντήριες οδηγίες (NCCN Guidelines/National Comprehensive Cancer Network Guidelines/Εθνικές κατευθυντήριες γραμμές για τον καρκίνο)
Χημειοθεραπεία, δίνεται σε όλες τις ασθενείς με όγκους μεγαλύτερους από 1cm. Εξαίρεση αποτελούν κάποιοι ειδικοί ιστολογικοί τύποι. Χημειοθεραπεία γίνεται για όγκους 0.6-1.0cm, μόνο σε δυσμενείς ιστολογικούς τύπους (GII&III, LVI, HER-2+). Η Trastuzumab γίνεται για όγκους HER-2+ μεγαλύτερους από 1cm ή σε θετικούς λεμφαδένες.
–Κατευθυντήριες οδηγίες ST. GALLEN
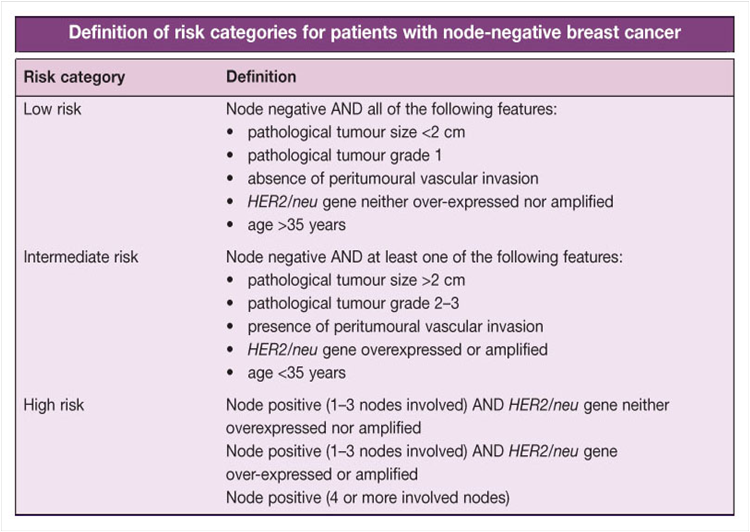
Οι γυναίκες με πρώιμο καρκίνο μαστού (χειρουργήσιμο) κατατάσσονται σε 3 κατηγορίες, ανάλογα με τον κίνδυνο υποτροπής:
- Χαμηλού κινδύνου.
- Μετρίου κινδύνου.
- Υψηλού κινδύνου.
-Το πρόγραμμα CMF/cyclophosphamide, methotrexate and fluorouracil/κυκλοφωσφαμίδη, μεθοτρεξάτη και φθοριοουρακίλη
Πατήστε, εδώ, για να διαβάσετε για την cyclophosphamide και τις παρενέργειές της
Πατήστε, εδώ, για να διαβάσετε για τη methotrexate και τις παρενέργειές της
Πατήστε, εδώ, για να διαβάσετε για τη fluorouracil και τις παρενέργειές της
Όφελος στο DFS (ελεύθερη νόσου επιβίωση) και OS (ολική επιβίωση) μετά 30 έτη παρακολούθησης. Χρησιμοποιείται, ακόμα, σε ασθενείς με αρνητικούς λεμφαδένες και σε αντενδείξεις ανθρακυκλινών. (Bonadonna et al. BMJ 2005; 330:217)
-ΧΜΘ με βάση τις ανθρακυκλίνες
Σύμφωνα με την ΕBCTCG, μετα-ανάλυση υπήρξε 26% μείωση των θανάτων σε νεαρές ασθενείς από καρκίνο μαστού. Το όφελος παρέμεινε για 15 έτη. Έτσι, οι ανθρακυκλίνες αποτελούν τμήμα της βασικής θεραπείας και χορηγούνται σε όλους τους ασθενείς, που πρέπει να λάβουν επικουρική θεραπεία, όταν δεν υπάρχουν συγκεκριμένες αντενδείξεις, π.χ. καρδιοπάθεια. Όλα τα προγράμματα ανθρακυκλινών δεν είναι ταυτόσημα. Προσοχή στις μακροπρόθεσμες συνέπειες, όπως τη λευχαιμία, τη συμφορητική καρδιοπάθεια και την πρώιμη εμμηνόπαυση.
Πατήστε, εδώ, για να διαβάσετε για τις ανθρακυκλίνες και τις παρενέργειές της
-Taxanes ως adjuvant θεραπεία:
Paclitaxel: Τα προγράμματα με πακλιταξέλη (AC->Paclitaxel) υπερτερούν από τα (υποβαθμισμένα) AC προγράμματα (;). Δεν έγινε σύγκριση με ιδιαιτέρως ισχυρά προγράμματα. Έχουν μεγαλύτερη διάρκεια, άρα περισσότερη τοξικότητα. Η απόλυτη διαφορά ήταν
– 5-έτη DFS: 4%-5%.
– 5-έτη OS: 0%-3%.
Πατήστε, εδώ, για να διαβάσετε για την πακλιταξέλη και τις παρενέργειές της (μη εγκεκριμένο πια)
Taxotere : Τα προγράμματα δοσεταξέλης υπερτερούν των ικανών προγραμμάτων με ανθρακυκλίνες (πχ FAC?; FEC100). Έχουν ίδια διάρκεια αλλά μεγαλύτερη τοξικότητα με TAC. Ολιγότερη τοξικότητα έχουμε με FECx3 ->Taxoterex3. Απόλυτη διαφορά
– 5-έτη DFS: 5%-7%.
– 5-έτη OS: 4%-6%.
Πατήστε, εδώ, για να διαβάσετε για την ταξοτέρη και τις παρενέργειές της
Για ασθενείς με θετικούς λεμφαδένες, το πρόγραμμα AC x 4 + Taxol x 4 είναι το ενδεδειγμένο. Ομοίως και το TAC x 6.
H διχογνωμία, όμως, παραμένει, λόγω της υποδοσολογίας των ασθενών της ομάδας ελέγχου.
Σηπτικοί θάνατοι, νευροτοξικότητα καρδιοτοξικότητα, οξεία λευχαιμία, τυφλίτιδα πρέπει να λαμβάνονται σοβαρά υπόψη.
Δεν είναι γνωστό το καλύτερο πρόγραμμα, η δοσολογία και ο παράγων (ταξάνη).
Υπάρχει ερώτημα για τους ασθενείς με θετικούς ορμονικούς υποδοχείς (ER+).
Όσο αφορά την εντατικοποίηση της θεραπείας, θα λέγαμε ότι η επαύξηση των δόσεων έχει όρια.
Άρα συμπερασματικά, ο ρόλος των ταξανών είναι αποδεδειγμένος, αλλά, πολλοί ισχυρίζονται, ότι το όφελος είναι μικρό μπροστά στις παρενέργειες. Η εντατικοποίηση των δόσεων έχει σημασία. Η υποστηρικτική αγωγή με αυξητικούς παράγοντες των λευκών και της ερυθράς σειράς βελτιώνει την έκβαση. Η κάθε 2 εβδομάδες A/C ->P είναι καλύτερη από το κάθε 3. Οι περισσότερες μελέτες δεν έλεγξαν, επαρκώς, την ένταση της δόσεως. Κάθε πρόγραμμα έχει ανάγκη ελέγχου.
Δεν είναι σαφές το όφελος κάθε ομάδας…αναμένονται τα στοιχεία της έκφρασης των γονιδίων…. Κάθε χρόνο, ανακαλύπτονται καινούρια φάρμακα. Η διάρκεια της χημειοθεραπείας είναι 6 έως 8 μήνες. Οι παρενέργειές της είναι: αναιμία, ευαισθησία στις λοιμώξεις, ανορεξία, αδυναμία, ναυτία, εμετοί, διάρροιες, στοματίτιδα, αλωπεκία.
-Όταν η θεραπευτική απόφαση είναι η ιστολογική εξέταση
Το ΗΕR-2 είναι ογκογονίδιο, που δίνει σήμα πολλαπλασσιασμού προς τον πυρήνα των κυττάρων. Υπερέκφραση του ΗΕR-2 σε κύτταρα καρκίνου μαστού δείχνει επιθετικότερη βιολογική συμπεριφορά και μικρότερη επιβίωση. Η Trastuzumab (HERCEPTIN) είναι εξανθρωποποιημένο μονοκλωνικό αντίσωμα αντι-HER2, που συνδέεται εκλεκτικά με το αντιγόνο HER2 στην επιφάνεια των καρκινικών κυττάρων και αναστέλλεται το σήμα πολλαπλασσιασμού των κυττάρων αυτών.
Η θέση του Herceptin σε HER2+ όγκους (NCCTG N 9831, NSABP B-31, BCIRG 006 HERA)
- DFS είναι στατιστικά σημαντικώς καλύτερο για τις ασθενείς, που έλαβαν 9 εβδομάδες το trastuzumab, έναντι αυτών, που δεν πήραν.
- OS καλύτερο στις ομάδες trastuzumab, έναντι όχι trastuzumab.
Υπάρχουν, βέβαια, ορισμένα αναπάντητα ερωτήματα, που αφορούν το βέλτιστο τρόπο χορήγησης trastuzumab, τη διάρκεια χορήγησης, τη μακροχρόνια αποτελεσματικότητα και τη μακροχρόνια τοξικότητα.
Το HERCEPTIN είναι ένα έξυπνο φάρμακο. Η υπερέκφραση ΗΕR-2 δίνει τη δυνατότητα χρησιμοποίησης του αντι- ΗΕR-2 μονοκλωνικού αντισώματος. Απ΄το FDA έχει εγκριθεί για τον μεταστατικό καρκίνο μαστού, αλλά και σε συμπληρωματική θεραπεία σε ασθενείς, που υπερεκφράζουν το ΗΕR-2.
Αλήθεια είναι αυτό, που περιμέναμε...;

Η σημασία της γονιδιακής υπογραφής
Γονιδιακή υπογραφή (Οι συγκεκριμένες εξετάσεις είναι αξιόπιστες; Δίνονται τα αποτελέσματα με τις μεταλλάξεις γονιδίων;)
- ONCOTYPE DX (21 γονίδια) (formalin-fixed, paraffin-embedded tissues)
Έλεγχος για υπερέκφραση σε ασθενείς με ER + όγκους (κίνδυνος υποτροπής της νόσου). Οι χαμηλού και ενδιάμεσου κινδύνου δεν έχουν όφελος από τη ΧΜΘ.
- MAMMAPRINT ASSAY Amsterdam (70 γονίδια) (limited by requirement for fresh frozen samples)
Έλεγχος, σε γυναίκες νεώτερες των 55 ετών με στάδιο Ι ΚΑΙ ΙΙ με αρνητικούς λεμφαδένες. Αναγνωρίζει ομάδες χαμηλού κινδύνου, με εξαιρετική πρόγνωση χωρίς ΧΜΘ.
Η χημειοθεραπεία έχει πολλές παρενέργειες….
Στο ερώτημα, μέχρι ποια ηλικία χορηγείται adjuvant Χημειοθεραπεία απαντά το Early Breast Cancer Trialists Collaborative Group (1998), που αποδεικνύει μείωση των ετησίων υποτροπών από τη χορήγηση συνδυασμένης ΧΜΘ
- Ηλικία μικρότερη των 40, 40%.
- Ηλικία 60-69, 16%.
- Ηλικία 70+ (δεν υπάρχουν δεδομένα).
Πράγματι, χρειάζονται οι ανθρακυκλίνες ή μπορούν να αντικατασταθούν από ισοδύναμα προγράμματα;
Η TOPO II A είναι δείκτης για όφελος από την θεραπεία με ανθρακυκλίνες. Ασθενείς με υπερέκφραση ή απουσία TOPO II A είχαν όφελος από τις ανθρακυκλίνες έναντι του CMF. Οι ασθενείς με φυσιολογικά αντίγραφα TOPO II A δεν είχαν επιπρόσθετο όφελος από την θεραπεία με ανθρακυκλίνες έναντι του CMF.
Έχει σημασία η ορμονοευαισθησία για τη χημειοθεραπεία;
Οι γυναίκες με αρνητικούς ορμονικούς υποδοχείς (ΕR-) ανταποκρίνονται καλύτερα στη ΧΜΘ (ΝSABP B-20, INT 100, CALGB, EBCTCG).
ASCO 2008 ΤΡΙΠΛΑ ΑΡΝΗΤΙΚΟΙ ΟΓΚΟΙ
Είναι ετερογενής ομάδα. Υπάρχουν πολλές πιθανές λύσεις αλλά καμιά ασφαλής επιλογή, όπως ανθρακυκλίνες, ταξάνες, σισπλατίνη, αναστολείς του PARP/poly-ADP/Adenosine diphosphate ribose polymerase. Αυτές οι ασθενείς, συνήθως, είναι φορείς του BRCA/BReast CAncer gene/Γονίδιο Καρκίνου του Μαστού.
Πατήστε, εδώ, για να διαβάστε για τη σισπλατίνη και τις παρενέργειές της
Πατήστε, εδώ, για να διαβάσετε για τους αναστολείς PARP και τις παρενέργειές τους
Η ορμονοθεραπεία ως συστηματική επικουρική θεραπεία στον πρώιμο καρκίνο του μαστού
Οι ορμόνες είναι γνωστό, ότι επηρεάζουν τους μαστούς.
Η ταμοξιφένη για 5 έτη έχει σαν αποτέλεσμα βελτίωση του DFS. Η χορήγηση ταμοξιφένης για 5 έτη παρέμεινε η στάνταρτ επικουρική ορμονοθεραπεία, για πολλά χρόνια. Περίπου ½ από τις αναμενόμενες υποτροπές και ⅔ από τους αναμενόμενους θανάτους συνέβησαν μετά από 5 έτη ταμοξιφένης. Ο μεγαλύτερος κίνδυνος υποτροπής υπάρχει τα 2 πρώτα χρόνια μετά το χειρουργείο.
Υπάρχει ανάγκη ανάπτυξης νέων φαρμάκων για να υπερνικηθεί η αντίσταση στην ταμοξιφένη.
Πατήστε, εδώ, για να διαβάσετε για την ταμοξιφένη και τις παρενέργειές του
Όσον αφορά τη θεραπευτική απόφαση των ορμονικών υποδοχέων, ισχυριζόμαστε, ότι υπάρχουν ευτυχώς νέα φάρμακα ορμονοθεραπείας οι αναστολείς αρωματάσης. Σε μεταεμμηνοπαυσιακές γυναίκες, με θετικούς ορμονικούς υποδοχείς, η χορήγηση αναστολέων αρωματάσης αποτελεί μαζί με την ταμοξιφένη τη μόνη συμπληρωματική θεραπεία. Οι σύγχρονες στρατηγικές είναι αντί για ταμοξιφένη χορήγηση του αναστολέα της αρωματάσης για 3-5 χρόνια ή 5 χρόνια ταμοξιφένη και μετά αναστολέας της αρωματάσης ή 2-3 χρόνια ταμοξιφένη και μετά αναστολέας της αρωματάσης μέχρι τα 5 χρόνια και κατά άλλους και περισσότερα.
Οι αναστολείς αρωματάσης είναι η λετροζόλη, η αναστραζόλη και η εξεμεστάνη. Χρησιμοποιούνται, γιατί έχουν διαφορετικό τρόπο δράσης από την ταμοξιφένη και υποδειγμένη υπεροχή η ισοδυναμία με την ταμοξιφένη.
– Πρώτη γραμμή στην μεταστατική νόσο
– Letrozole, anastrozole, exemestane καλύτερες από progestins and tamoxifen
– Προεγχειρητική θεραπεία.
– Letrozole καλύτερη από tamoxifen.
– Anastrozole ισοδύναμη με την tamoxifen.
Πατήστε, εδώ, για να διαβάσετε για τη λετροζόλη και τις παρενέργειές της
Πατήστε, εδώ, για να διαβάσετε για την εξεμεστάνη και τις παρενέργειές της
Πατήστε, εδώ, για να διαβάσετε για την αναστραζόλη και τις παρενέργειές της
Οι αναστολείς της αρωματάσης είναι σημαντική adjuvant ενδοκρινική θεραπεία σε μεταεμμηνοπαυσιακές γυναίκες. Διαφορές στην αποτελεσματικότητα ανάμεσα στους αναστολείς αρωματάσης απαιτεί επιβεβαίωση με μελέτες. Οι ανεπιθύμητες ενέργειες, γενικά, είναι πιο αντιμετωπίσιμες και προβλέψιμες από αυτές της ταμοξιφένης. Μελέτες θα προσδιορίσουν την καλύτερη χρήση των AIs στην επικουρική θεραπεία.
Και τώρα η κριτική της θεραπευτικής απόφασης
Η θεραπευτική απόφαση είναι προϊόν επεξεργασίας των κριτηρίων, πολλά από τα οποία καθορίζουν την πρόγνωση. Η επίπτωση του καρκίνου του μαστού αυξάνει. Αλλά και τα ποσοστά ίασης βελτιώνονται. Η νόσος εξακολουθεί να προσβάλλει τις γυναίκες. Πιστεύεται, ότι οι μελλοντικές ανακαλύψεις για τον καρκίνο του μαστού θα εστιαστούν σε μοριακά δεδομένα. Νέα έξυπνα φάρμακα προστίθενται στο οπλοστάσιο μας. Το μέλλον διαφαίνεται αισιόδοξο…

ΠΑΡΑΚΟΛΟΥΘΗΣΗ ΑΣΘΕΝΩΝ ΜΕ ΠΡΩΙΜΟ ΚΑΡΚΙΝΟ ΜΑΣΤΟΥ ΜΕΤΑ ΤΗΝ ΑΡΧΙΚΗ ΘΕΡΑΠΕΙΑ
- Ιστορικό/ Σύμπτωμα.
- Φυσική εξέταση.
- Αυτοεξέταση μαστού.
- Μαστογραφία.
- Εκπαίδευση ασθενούς για τα συμπτώματα υποτροπής.
- Συντονισμός φροντίδας υγείας.
- Εξέταση πυέλου.
Φυσική εξέταση:
Κάθε 3-6 μήνες τα πρώτα 3 χρόνια. Κάθε 6-12 μήνες τα επόμενα 2 χρόνια.
Στη συνέχεια κάθε χρόνο.
- Αυτοεξέταση μαστού: Κάθε μήνα.
- Μαστογραφία: Γενικά, κάθε χρόνο. Μετά συντηρητική επέμβαση, σε 6 μήνες μετά ακτινοθεραπεία, ύστερα ανά έτος. Επί σταθεροποιήσεως των ευρημάτων ανά έτος. Έχει ακτινοβολία και προκαλεί καρκίνο. Καλύτερα να μη γίνεται.
- Τοπική υποτροπή είναι η ανάπτυξη καρκίνου στο σύστοιχο μαστό, μετά την αρχική θεραπεία. Μπορεί να είναι το μόνο εύρημα ή να υπάρχει συνύπαρξη με μεταστάσεις. Η πρώιμη ανεύρεση μπορεί να συνεπάγεται ίαση. Προσοχή στα 2 πρώτα χρόνια!!!
- Εξέταση πυέλου: Πρέπει να γίνεται τακτικός γυναικολογικός έλεγχος και να ελέγχεται το πάχος ενδομητρίου ειδικά επί λήψεως Tamoxifen. Οι εξετάσεις πρέπει να είναι αραιότερες, αν έχει προηγηθεί υστερεκτομή ή ωοθηκεκτομή.
- Γενική εξέταση αίματος: Δεν υπάρχουν επαρκή δεδομένα, γι’ αυτό δε συνίσταται σα μέθοδος ρουτίνας.
- Βιοχημικός έλεγχος, έλεγχος νεφρικής ή ηπατικής λειτουργίας: Δεν υπάρχουν επαρκή δεδομένα, γι’ αυτό δεν συνιστώνται σα μέθοδοι ρουτίνας.
- Καρκινικοί δείκτες (CE15-3, CEA, CA27-29): Δεν υπάρχουν επαρκή δεδομένα, γι’ αυτό δεν συνιστώνται σα μέθοδοι ρουτίνας.
Σταματήστε, να ασχολείστε με τους καρκινικούς δείκτες. Δεν έχουν καλή ευαισθησία και ειδικότητα
Απεικονιστικές μέθοδοι:
- Α/Α θώρακος.
- Υπερηχογράφημα ήπατος – χοληφόρων.
Για το σπινθηρογράφημα οστών, τις αξονικές τομογραφίες θώρακος, άνω & κάτω κοιλίας, εγκεφάλου, τη μαγνητική τομογραφία και το PET/ CT δεν υπάρχουν επαρκή δεδομένα και γι’ αυτό δε συνιστώνται σα μέθοδοι ρουτίνας, παρά μόνο επί ενδείξεων.
ΕΠΙΜΟΡΦΩΤΙΚΟΣ ΟΔΗΓΟΣ ΓΙΑ ΤΟΝ ΚΑΡΚΙΝΟ ΤΟΥ ΜΑΣΤΟΥ
Ο καρκίνος του μαστού προσβάλλει χιλιάδες γυναίκες κάθε έτος. Η πραγματική αιτία του καρκίνου του μαστού δεν είναι ακόμη γνωστή, γι’ αυτό η πρόληψη είναι το κλειδί, αφού πολλοί παράγοντες αυξάνουν τον κίνδυνο.
Οι παρακάτω οδηγίες είναι σημαντικές και σε καμιά περίπτωση δεν αντικαθιστούν την έμπειρη συμβουλή του ογκολόγου.
- Το screening, όπως το υπερηχογράφημα μαστών και η αυτοεξέταση μπορεί να βοηθήσουν στην πρώιμη διάγνωση.
Screening for Breast Cancer, JAMA. 2005;293:1245-1256.
- Αν έχετε κληρονομικό ιστορικό, το γενετικό τεστ μπορεί να βοηθήσει (μην ασχολείστε).
BRCA1 testing in families with hereditary breast- ovarian cancer. A prospective study of patient decision making and outcome. JAMA. 1996;257:24.
- Αποφύγετε την παχυσαρκία.
Adult Weight Change and Risk of Postmenopausal Breast Cancer. JAMA. 2006;296:193-201.
- Αποφύγετε την υπερβολική λήψη οινοπνεύματος.
Alcohol and Breast Cancer. Review of Epidemiologic and Experimental Evidence and Potential Mechanisms. JAMA. 2001;286:2143-2151.
- Κάντε άσκηση τακτικά, 4 ή περισσότερες ώρες την εβδομάδα, για να ελαττώσετε τα επίπεδα των ορμονών σας.
Recreational physical Activity and the Risk of Breast Cancer in Postmenopausal Women. JAMA. 2003;290q1331-1336.
- Σε περίπτωση, που υποβληθείτε σε ακτινοθεραπεία (π.χ. Hodgkin’s λέμφωμα), ρωτήστε αν η περιοχή των μαστών θα προστατευθεί.
Effect of Chest X-Rays on the Risk of Breast Cancer Among BRCA1/2 Mutation Carriers in the International BRCA1/2 Carrier Cohort Study. Journal of Clinical Oncology, 10. 1200/JCO.2005.03.3126.
- Τα οιστρογόνα με προγεστίνη (θεραπεία με οιστρογόνα, αντισυλληπτικά, στειρότητα, εγκυμοσύνη σε μεγάλη ηλικία, εμμηνόπαυση) μπορεί σε μερικές περιπτώσεις ν’ αυξήσουν τον κίνδυνο.
Menopausal Estrogen and Estrogen-Progestin Replacement Therapy and Breast Cancer Risk. JAMA.2000;283:485-491.
- Μετά την εμμηνόπαυση μερικές θεραπείες (SERMs/Selective estrogen receptor modulators/Εκλεκτικοί ρυθμιστές υποδοχέων οιστρογόνων-tamoxifen, Αναστολείς αρωματάσης) μειώνουν τον κίνδυνο. Χρησιμοποιήστε τις, μόνο με ένδειξη του ογκολόγου, γιατί έχουν πάρα πολλές ανεπιθύμητες ενέργειες. Υπάρχουν και φυσικές θεραπείες, χωρίς παρενέργειες.
Tamoxifen and Breast Cancer Incidence Among Women With Inherited Mutations in BRCA1 and BRCA2. JAMA. 2001;286:2251-2256.
- Η επίδραση των περιβαλλοντολογικών παραγόντων (χημικά, μέταλλα, μόλυνση ατμόσφαιρας και σκόνη) στον κίνδυνο για καρκίνο του μαστού είναι σημαντική.
Breast Cancer and Risk Factor. Breast Cancer Center. University Californy San Francisco. UCSF.
ΑΝ ΣΟΥ ΣΥΜΒΕΙ……
να θυμώσεις,
πρέπει,
αλλά να μην εξαντλήσεις τον θυμό στο ασήμαντο…
δώσ’ του φτερά να μετουσιωθεί σε κάτι παραπάνω
σε επιστήμη,
τέχνη,
αγάπη,
ότι σου είναι δυνατόν…
Ρέα Γαλανάκη
Τολμήστε και ζήστε!
Απαιτούνται ριζικές αλλαγές στη θεραπεία του καρκίνου του μαστού!!!
Να προτιμάτε τις φυσικές θεραπείες για τον καρκίνο του μαστού, σύμφωνα με το Μοριακό Προφίλ του Όγκου
Η ζωή είναι πολύτιμη.
Η ζωή είναι δική σας. Πάρτε την στα χέρια σας!
Το μοριακό προφίλ του όγκου είναι απαραίτητο και χρήσιμο εργαλείο για τη θεραπευτική σας απόφαση.
Ζητείστε την εξέταση πριν κάνετε οποιαδήποτε θεραπεία. Η ζωή σας είναι πολύτιμη.
Ζητήστε από την EMEDI πληροφορίες για το μοριακό προφίλ του όγκου.
Γράφει η
Δρ Σάββη Μάλλιου Κριαρά
Ειδικός Παθολόγος- Ογκολόγος, MD, PhD
Διαβάστε περισσότερα για την Σάββη Μάλλιου Κριαρά
Εμπιστευθείτε τους διατροφικούς συμβούλους της EMEDI
Εμπιστευθείτε το ογκολογικό συμβούλιο της EMEDI
Τα κατάλληλα συμπληρώματα διατροφής για τον καρκίνο μαστού
Πατήστε, εδώ, για να παραγγείλετε τα κατάλληλα συμπληρώματα διατροφής για τον καρκίνο μαστού
Η καθοδήγηση για την επιλογή των ποιων συμπληρωμάτων διατροφής, από τα ανωτέρω, είναι κατάλληλα για την ασθένειά σας θα γίνει σε συνεννόηση με το θεράποντα ιατρό.
Διαβάστε, επίσης,
Η καρδιοτοξικότητα από τα χημειοθεραπευτικά φάρμακα
Αποφύγετε την ορμονοθεραπεία στην εμμηνόπαυση
Αντικαρκινικό φυτό για χημειοθεραπεία
Τα νέα για τον καρκίνο του μαστού
Η νανοϊατρική στον καρκίνο του μαστού
European Society for Medical Oncology